Гост 19710-83 этиленгликоль. технические условия (с изменениями n 1, 2, 3)
Содержание:
- Этиленгликоль – токсичный двухатомный спирт
- В каких сферах применяется?
- Что такое этиленгликоль
- Как разводить антифриз концентрат: таблица значений
- Теплоноситель – основные требования в системе отопления
- Что такое пропиленгликоль?
- Производство
- Этиленгликоль. Свойства, характеристики и определение этиленгликоля
- Последствия и осложнения отравления
- Пропиленгликоль или этиленгликоль: сравнение теплоносителей
Этиленгликоль – токсичный двухатомный спирт
Химическая формула данного простейшего многоатомного спирта – С2Н6О2 (иначе ее можно записать следующим образом – НО–СН2–СН2–ОН). Этиленгликоль имеет слегка сладковатый вкус, не имеет запаха, в очищенном состоянии выглядит, как немного маслянистая бесцветная прозрачная жидкость.
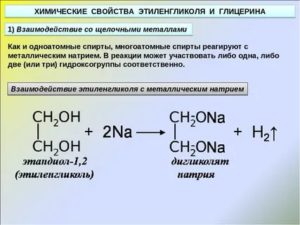
Так как он причислен к токсичным соединениям (по общепринятой классификации – третий класс опасности), следует избегать попадания данного вещества (в растворах и в чистом виде) в организм человека. Основные химические и физические свойства 1,2-диоксиэтана:
- молярная масса – 62,068 г/моль;
- коэффициент оптического преломления – 1,4318;
- температура воспламенения – 124 градуса (верхний предел) и 112 градусов (нижний предел);
- температура самовоспламенения – 380 °С;
- температура замерзания (стопроцентный гликоль) – 22 °С;
- температура кипения – 197,3 °С;
- плотность – 11,113 г/кубический сантиметр.
Пары описываемого двухатомного спирта вспыхивают в тот момент, когда его температура достигает 120 градусов. Еще раз напомним, что 1,2-этандиол имеет 3-й класс опасности. А это означает, что его предельно допустимые концентрации в атмосфере могут быть не более 5 миллиграмм/кубический метр. Если же этиленгликоль попадает в организм человека, в нем могут развиться необратимые негативные явления, которые способны привести к смерти. При однократном употреблении вовнутрь 100 и более миллилитров гликоля наступает летальный исход.

Пары данного соединения менее токсичны. Так как этиленгликоль характеризуется сравнительно малым показателем летучести, реальная опасность для человека возникает тогда, когда он систематически вдыхает пары 1,2-этандиола. О том, что есть вероятность отравления парами (либо туманами) рассматриваемого соединения, сигнализирует кашель и раздражение слизистой оболочки. Если человек отравляется гликолем, ему следует принять препарат, содержащий 4-метилпиразол (мощный антидот, подавляющий фермент алкогольдегидрогеназы), или этанол (одноатомный этиловый спирт).
В каких сферах применяется?
Пропиленгликоль используется:
в промышленности – в роли:
теплоносителя, защищатющего от коррозии под давлением, растворяющего активные вещества и контролирующего вязкость. Пропиленгликлолевый теплоноситель устойчив к разложению и окислению в период эксплуатации при температуре от -60оС до +110оС, а также позволяет ему на 25% снижать гидродинамичное сопротивление
Поэтому использование его важно, к примеру, в отопительных системах. Теплоноситель позволяет насосам во вторичном контуре работать эффективней, а также помогает удалять отложения и накипь с поверхности труб и котла даже при аварийном отключении системы;
важного ингредиента для покрытий и красок (в том числе печатных), растворителей, жидких моющих средств и антифризов, противообледенителей летательных аппаратов;
строительного материала – ненасыщенных полиэфирных смол, без которых немыслимо производство мебели, синтетических и гелевых покрытий, морских конструкций.
Используют его и в промышленности текстильной, когда производят полиэфирные волокна.
Также здесь необходимо напомнить про его полимер полипропиленгликоль, без которого немыслимо производство полиуретанов, гидравлических жидкостей, смазок и загустителей;
в пищевой промышленности
Тот, кто, приобретая продукты, внимательно изучал их состав, вероятно, встречался с обозначением E1520. Это и есть пропиленгликоль, необходимый как консервант, а также диспергирующий, смягчающий и влагоудерживающий агент. В быту известный как стабилизатор, загуститель и подсластитель. И признанный в том числе управлением по контролю за качеством и пищевых продуктов и лекарственных препаратов США;
в жидкости электронных сигарет. Здесь он играет роль связующего элемента для глицерина и никотина. Также вещество позволяет имитировать дым, что может быть очень важно для пожарных учений или театральных простановок;
в косметике. Здесь можно вспомнить производный от него пентиленгликоль, благодаря которому её активные ингредиенты увеличивают свою биодоступность, усиливается её водостойкость и способность удерживаться на коже. К тому же пропиленгликоль входит в состав продуктов личной гигиены – мягких, однородных и влажных: дезодорантах, лосьонах для тела, солнцезащитных кремах, кремах для лица, шампунях, губных помадах. Здесь ему отводится функция эксципиента – неактивного активирующего вещества, помогающего сохранить запах;
в лекарствах. Здесь в первую очередь надо вспомнить про фармацевтический пропиленгликоль USP/EP, играющем роль эксципиента, входящего в состав гелевых капсул и сиропов от кашля. Применяется пропиленгликоль и как растворитель. Известно, что в составе инъекционных препаратов его порядка 40%.
Казалось бы, от этого химического соединения сплошная польза. Но всё не так просто. Нельзя упускать из виду вредный побочный эффект.

Что такое этиленгликоль
По определению этиленглико́ль (гликоль, 1,2-диоксиэтан, этандиол-1,2) — кислородсодержащее органическое соединение, двухатомный спирт, простейший представитель многоатомных спиртов. Если вещество очищено, то представляет собой прозрачную бесцветную жидкость маслянистой консистенции.
Изначально этиленгликоль использовался во времена Первой мировой войны в качестве глицерина. Однако со временем изменил свое направление. Его стали использовать в различных сферах химической промышленности.

Формула и класс вещества
Химическая формула гликоля — C2H6O2, рациональная — C2H4 (OH) 2, структурная — HO—CH2—CH2—OH . В основе молекулы лежит непредельный скелет этилена, который состоит из двух атомов карбона. На свободные валентные места присоединились две гидроксильные группы.
У этиленгликоля есть несколько названий, которые зачастую встречаются в составе продуктов химического производства:
- гликоль;
- этандиол-1,2;
- 1,2-диоксиэтан.
Молекула имеет подобие транс-конфигурации в размещении гидроксильных групп. Такое расположение соответствует самому удаленному расположению водородов, что дает максимальную устойчивость системы.
Как получают
Массовое получение 1.2-этандиола началось еще в тридцатые годы прошлого века. Сначала получали лишь одним методом, потом появились новые. Таким образом, гликоль можно получить несколькими способами, однако некоторые из них стали частью истории, а другие превзошли их качеством.
Изначально 1,2-диоксиэтан получали из дибромэтана. Двойная связь этилена разрывается, а свободные валентности занимаются галогенами — исходным веществом в данной реакции. Образование промежуточного соединения возможно благодаря замещению ацетатными группами, которые при гидролизе превращаются в спиртовые.
С улучшением технологий появился новый метод — получение этиленгликоля прямым гидролизом любых этанов и этиленов , которые замещены двумя галогенами соседних атомов карбона. С помощью различных водных растворов, карбонатов металлов, воды и диоксида свинца начинается реакция, которая возможна лишь при больших температурах и давлении. Побочные вещества — диэтиленгликоль и триэтиленгликоль.
Следующий способ позволил получать 1,2-диоксиэтан из эфира этиленхлоргидрина путем его гидролиза угольными солями. При 170 градусах выход целевого продукта достигал 90 %. Однако был значительный недостаток — гликоль необходимо извлекать из раствора соли. Ученые решили эту проблему. Они разбили процесс на две стадии, при этом оставив то же исходное вещество.
Гидролиз этиленгликоль ацетатов стал отдельным способом, когда получилось добыть исходный реагент путем окисления этилена в уксусной кислоте кислородом.

Как разводить антифриз концентрат: таблица значений
Если антифриз концентрат сертифицирован и выпущен на рынок, на упаковке с ним будет написана подробная инструкция, как его разводить с дистиллированной водой. В данном случае ориентироваться нужно на климатическую зону, в которой эксплуатируется машина. Если температура в холодное время года редко понижается ниже минуса 20 градусов по Цельсию, не имеет смысл разводить антифриз на работу при температуре меньше минуса 40 градусов по Цельсию.
Приведем некоторые стандартные значения приготовления антифриза из концентрата:
— 25 градусов по Цельсию: концентрат смешивается с водой в пропорции 2 к 3, то есть 2 мерных объема концентрата к 3 мерным объемам вода
Важно отметить, что порог закипания в таком случае снизится примерно до +130 градусов по Цельсию;
— 45 градусов по Цельсию: концентрат смешивается с водой в пропорции 1 к 1, например, 1 литр воды на 1 литр концентрата антифриза.. Ориентироваться при смешивании охлаждающей жидкости можно на следующие значения:
Ориентироваться при смешивании охлаждающей жидкости можно на следующие значения:
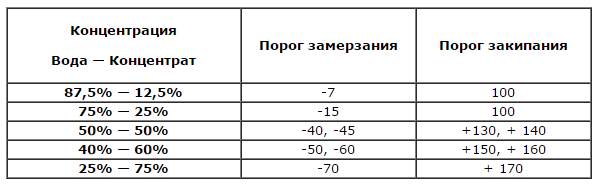
Обратите внимание, что в данном случае не работает принцип «чем больше воды, тем ниже температура замерзания». Разбавлять концентрат антифриза необходимо в пропорциях, приведенных в таблице
Если налить слишком много воды, охлаждающая жидкость потеряет свойства противостояния низким температурам.
Незаменимым компонентом системы охлаждения автомобиля является антифриз или тосол. Эта жидкость отличает то, что она закипает и замерзает при повышенных и пониженных температурах. Чаще всего антифриз можно купить уже в готовом виде, но некоторые автолюбители предпочитают самостоятельно разводить концентрат, да и готовые составы обычно способны выдерживать слишком экстремально низкие температуры, поэтому вполне логично делать смеси. Так как в состав всех хладагентов входит вода, то ей можно разбавлять охладительную жидкость, единственное, что использовать для этой цели можно исключительно дистиллированную воду. В противном случае из-за магния и кальция, которым богата «живительная влага» из крана, в системе охлаждения автомобиля может образоваться накипь и осадок. Если же уверены что обычная вода не жесткая (не превышает 5 мг-экв/л), то можно разбавить антифриз и ей. Также воду можно проверить на наличие примесей самостоятельно. Для этого необходимо сделать раствор в небольшом количестве в прозрачной емкости и подождать некоторое время. Если на дне стакана, банки или бутылки образовался осадок, то такую жидкость лучше не использовать для смешивания.
Теплоноситель – основные требования в системе отопления
Какой же должен быть теплоноситель для системы автономного отопления? Попробуем сформулировать необходимые критерии соответствия «идеального» варианта.
- Начнем с того, что жидкость на отопление нам понадобится с максимально высокой теплоемкостью. Это условие необходимо для качественного аккумулирования и дальнейшей отдачи тепловой энергии посредством радиаторов.
- Нам понадобится теплоноситель, с химическим составом не активизирующим коррозионные процессы в котельном оборудовании, в разводке труб, отопительно-радиаторных, запорно-регулирующих и прочих конструкциях отопительной системы.
- Особые требования следует выдвигать к химической составляющей теплоносителя. Состав проходит через уплотнения насосного оборудования, и другие конструктивные элементы содержащие резиновые уплотнительные кольца и может подвергать их к разрушению.
- Одним из главных показателей, указывающих, что у вас в распоряжении качественный теплоноситель — широкий диапазон температурного использования. Производитель заботящийся о своей репутации предлагает теплоноситель с рабочими характеристиками, начиная от низких температурных значений кристаллизации до высоких пороговых значений закипания.
- Теплоноситель не должен содержать соль, которая так “любит” выпадать в виде накипи в теплообменнике, выводя его из строя, а также разрастаться твердыми отложениями во внутреннем сечении труб.
- Необходимо, чтобы теплоноситель для отопления обладал повышенной стабильностью. Нам потребуется теплоноситель, который не распадается со временем на составные части ни под воздействием высоких температур, ни под воздействием своего химического состава. На протяжении всего срока службы, теплоноситель обязан сохранять заявленные технические характеристики, такие как: плотность, текучесть, теплоемкость, химическая инертность.
- Кроме того, теплоноситель не должен угрожать здоровью жильцов в случае протечек. Не допускаются токсичные испарения. Жидкость применяемая в отоплении должна быть полностью негорючая и не образовывать взрывоопасных газовых смесей при испарении.
- Как правило, система отопления имеет значительные объемы, таким образом одним из немаловажных критериев для рачительного домовладельца становится приемлемая стоимость теплоносителя.
Что такое пропиленгликоль?
Как свидетельствует Википедия, это химическое вещество, образующееся в результате гидратации оксида пропилена – летучего соединения, обычно применяемого при создании полиуретанового пластика – при температуре 160-200С и давлении примерно 1,6 МПа. Помимо него в ходе данной реакции образуются дипропиленгликоль (13%) и трипропиленгликоль (1,5%). Вещество имеет и иное наименование – пропандиол-1,2.
Вещество представляет собой прозрачную бесцветную жидкость без ярко выраженного запаха и со сладковатым вкусом, чья плотность ниже, нежели у глицерина и этиленгликоля, но выше в сравнении с этанолом. При этом одноатомные спирты и этиленгликоль уступают веществу в вязкости.
В научной литературе описываются и иные методы получения пропиленгликоля. Например, при помощи гидратации аллилового спирта, восстановлении ацетола или глицидного спирта, гидрирования бутиллактата, гидрогенолиза глицеринов кокосового масла и пр. Химическая формула вещества – C3H8O2.
Пропиленгликоль прекрасно смешивается с водой, растворяет практически все низкомолекулярные органические соединения, содержащие кислород и азот. Способен поглощать из воздуха водяной пар. Эти замечательные свойства делают его востребованным во многих сферах.
Производство
Промышленные маршруты
Этиленгликоль получают из этилена (этена) через промежуточный оксид этилена . Оксид этилена реагирует с водой с образованием этиленгликоля в соответствии с химическим уравнением :
- С 2 Н 4 О + Н 2 О → НО-СН 2 СН 2 -ОН
Эта реакция может быть катализируемой с помощью либо кислот или оснований , или может иметь место при нейтральном значении рН при повышенных температурах. Наибольший выход этиленгликоля происходит при кислом или нейтральном pH с большим избытком воды. В этих условиях можно достичь выхода этиленгликоля 90%. Основными побочными продуктами являются олигомеры диэтиленгликоль , триэтиленгликоль и тетраэтиленгликоль . Разделение этих олигомеров и воды требует больших затрат энергии. Ежегодно производится около 6,7 млн тонн.
Более высокая селективность достигается за счет использования Shell «ы процесса OMEGA . В процессе OMEGA оксид этилена сначала превращается в диоксид углерода ( CO2) до этиленкарбоната . Затем это кольцо гидролизуют основным катализатором на второй стадии с получением моноэтиленгликоля с селективностью 98%. На этом этапе снова выделяется диоксид углерода, который может быть снова подан в технологический контур. Углекислый газ частично поступает из производства окиси этилена, где часть этилена полностью окисляется .
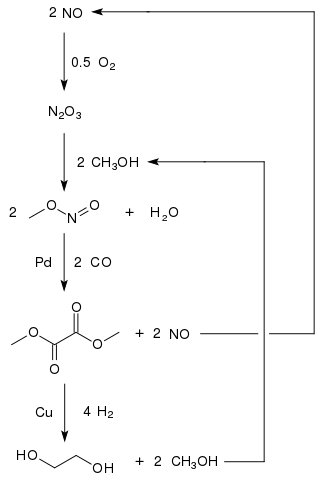
Этиленгликоль производится из окиси углерода в странах с большими запасами угля и менее строгими экологическими нормами. Окислительное карбонилирование метанола до диметилоксалата обеспечивает многообещающий подход к производству этиленгликоля на основе C 1 . Диметилоксалат может быть преобразован в этиленгликоль с высокими выходами (94,7%) путем гидрирования с медным катализатором:
Поскольку метанол перерабатывается, потребляются только окись углерода, водород и кислород. Один завод производственной мощностью 200 000 тонн этиленгликоля в год находится во Внутренней Монголии , а второй завод в китайской провинции Хэнань с мощностью 250 000 тонн в год был запланирован на 2012 год. По состоянию на 2015 год, четыре завода в Китае с производительностью 200 000 т / год каждая действовала, и, по крайней мере, еще 17 машин в будущем.
Биологические маршруты
У гусеницы большой восковой моли, Galleria mellonella , есть кишечные бактерии, способные разлагать полиэтилен (PE) до этиленгликоля.
Исторические маршруты
Согласно большинству источников, французский химик Шарль-Адольф Вюрц (1817–1884) впервые получил этиленгликоль в 1856 году. Сначала он обработал «иодид этилена» (C 2 H 4 I 2 ) ацетатом серебра, а затем гидролизовал полученный «диацетат этилена». с гидроксидом калия . Вюрц назвал свое новое соединение «гликоль», потому что он разделяет качества как этилового спирта (с одной гидроксильной группой), так и глицерина (с тремя гидроксильными группами). В 1859 году, Вюрец готовил этиленгликоль через гидратацию из окиси этилена . По всей видимости, до Первой мировой войны этиленгликоль не производился и не применялся в коммерческих целях , когда он был синтезирован из этилендихлорида в Германии и использовался в качестве заменителя глицерина во взрывчатых веществах .
В Соединенных Штатах полукоммерческое производство этиленгликоля через этиленхлоргидрин началось в 1917 году. Первый крупномасштабный промышленный завод по производству гликоля был построен в 1925 году в Южном Чарльстоне, Западная Вирджиния , компанией Carbide and Carbon Chemicals Co. (ныне Union Carbide Corp.) . К 1929 году этиленгликоль использовался почти всеми производителями динамита . В 1937 году компания Carbide запустила первую установку, основанную на процессе Лефорта, для парофазного окисления этилена до окиси этилена. Carbide сохраняла монополию на процесс прямого окисления до 1953 года, когда процесс научного проектирования был коммерциализирован и предложен для лицензирования.
Этиленгликоль. Свойства, характеристики и определение этиленгликоля
Определение этиленгликоля. Бесцветная сиропообразная сладковатая жидкость без запаха. Температура кипения 197,9°C; температура плавления 12,6°C. Смешивается с водой и спиртом. Порог восприятия запаха 1320 мг/л, привкуса 450 мг/л.
Этиленгликоль – Яд!
Токсическое действие этиленгликоля зависит от ряда обстоятельств: индивидуальной чувствительности организма; количества; состояния нервной системы; от степени наполнения желудка; наличия или отсутствия рвоты. Дозы, вызывающие смертельное отравление этиленгликолем варьируются в широких пределах – от 100 до 600 мл. По данным ряда авторов, смертельной дозой для человека является 50-150 мл. Смертность при поражении этиленгликолем очень высока и составляет более 60% всех случаев отравления. Механизм токсического действия этиленгликоля до настоящего времени изучен недостаточно. Этиленгликоль быстро всасывается (в том числе через поры кожи) и в течение нескольких часов циркулирует в крови в неизмененном виде, достигая максимальной концентрации через 2-5 часов. Затем его содержание в крови постепенно снижается, и он фиксируется в тканях. Характерно двухфазное действие яда. Первоначально проявляется наркотический эффект, что связано с действием на центральную нервную систему всей молекулы спирта(ЭГ), проявляющийся в состоянии опьянения и нарушения психической деятельности. Эти явления наблюдаются в течение 24-48 часов с момента отравления. При этом отмечается угнетение дыхания. Будучи сосудистым и протоплазматическим ядом, этиленгликоль вызывает отек, набухание и некроз сосудов. Результатом этого действия является кислородное голодание тканей мозга. Понижается кислородопереносящая функция гемоглобина. Нарушается обмен веществ с накоплением недоокисленных продуктов.
В ранние сроки отравления больные погибают от острой сердечной недостаточности или от отека легких.
Если отравленный вышел из стадии мозговых явлений, то дальнейшая симптоматика является результатом второй фазы токсического действия этиленгликоля, а именно результатом второй фазы токсического действия продуктов его окисления – щавелевой кислоты и её солей (щавелевого кальция).
Последний накапливается в мозгу, в почках и других органах. Происходит обеднение кальцием крови и тканей, что ведет к нарушению нервно-мышечной функции, нарушению свертываемости крови. Этиленгликоль ведет к усиленному распаду белков и глубокому изменению углеводного обмена.
Теплоносители на основе этиленгликоля
Вместе с тем, водные растворы этиленгликоля обладают удовлетворительными теплофизическими свойствами и получили широкое распространение в качестве автомобильных антифризов, позднее и бытовых антифризов для систем отопления.
Однако, при замене воды на этиленгликолевые антифризы необходимо помнить и об изменении коэффициента температуры расширения антифриза. Для Вашего удобства мы приводим зависимость расширительных баков от объема системы в таблице 1.
Табл. 1
|
Объем системы, л |
Объем расширительного бака, л |
|
|
вода |
этиленгликоль |
|
|
120 |
25 |
35 |
|
345 |
50 |
80 |
|
580 |
80 |
100 |
|
810 |
100 |
150 |
|
1155 |
150 |
200 |
|
1730 |
200 |
300 |
|
2310 |
300 |
500 |
|
2890 |
300 |
500 |
|
3470 |
500 |
2*300 |
Зависимость температуры замерзания теплоносителей от концентрации в них этиленгликоля:
Табл. 2
|
tзамерзания °С |
-40 |
-30 |
-20 |
-10 |
-5 |
|
|
содержание, % масс. |
53 |
46 |
36 |
24 |
14 |
1 |
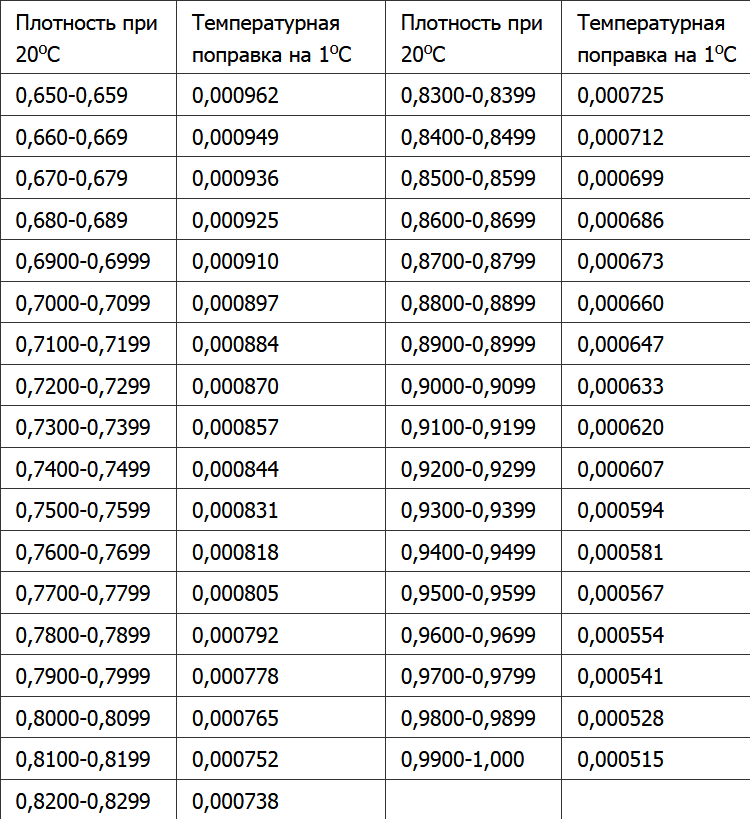
В домашних условиях можно определить температуру замерзания tзамерзания °С эксплуатируемого теплоносителя по плотности. Зависимость плотности от температуры замерзания для водных растворов этиленгликоля приведена в таблице 3.
Зависимость плотности от температуры замерзания этиленгликоля:
Табл. 3
|
tзамерзания °С |
-40 |
-30 |
-20 |
-10 |
-5 |
|
|
Плотность, кг/м3 |
1069 |
1060 |
1047 |
1030 |
1017 |
999,2 |
Возврат к списку
Последствия и осложнения отравления
К сожалению, последствия отравления этиленгликолем очень тяжелые. Около 40% больных, принявших его внутрь, погибают в течение 2-х недель.
Причиной летального исхода являются такие осложнения:
- Острая почечная недостаточность, уремия (отравление солями мочевой кислоты);
- Отек мозга;
- Отек легких;
- Отек оболочек сердца с его остановкой;
- Острый токсический гепатит с тяжелой недостаточностью функции.
Не угрожающие жизни осложнения часто приводят к инвалидности. К таким последствиям относятся: атрофия зрительных нервов, потеря зрения, хроническая сердечная, почечная недостаточность, цирроз печени, поражение центральной нервной системы в виде бессонницы, астении и даже психических расстройств.
Этиленгликоль – это яд, о чем всегда нужно помнить. Категорически нельзя употреблять его внутрь в любом количестве, а в случаях воздействия его паров надо обратиться к врачу токсикологу, пройти обследование, лечение и принять меры профилактики.
Пропиленгликоль или этиленгликоль: сравнение теплоносителей
Пропиленгликоль и этиленгликоль (этандиол-1,2) – это простейшие двухатомные спирты, получившие широкую популярность, наряду с глицерином, в качестве низкозамерзающих жидкостей (антифризов) в системах отопления.
Их отличает от других теплоносителей то, что они прекрасно выдерживают высокие температуры при соединении с водой и начинают закипать только при 105°С-110°С при нормальном атмосферном давлении и при 120°С-150°С – при повышенном. В зависимости от степени разведения, температура их кристаллизации составляет от -40°С до -70°С.
В их составе могут присутствовать антикоррозионные присадки для защиты внутренних элементов системы от коррозии и снижения пенообразования, что позволяет существенно увеличить ее срок эксплуатации.
Отличие этиленгликоля от пропиленгликоля
Тепло- и хладоносители на основе этилен гликоля (этандиола) отличаются более высокими теплоемкостью и теплопроводностью по сравнению с водными растворами монопропиленгликоля, а это позволяет применять в схемах радиаторы и теплообменники меньшего размера. Они также обладают более низкой вязкостью, что обеспечивает лучшую циркуляцию теплоносителя внутри системы и снижение гидродинамических потерь.
Благодаря малой вязкости этандиола на его основе можно создавать растворы различных концентраций с максимально низкой температурой кристаллизации -70°С. При этом есть еще и главное отличие – этиленглико ль стоит почти в 2 раза дешевле своего конкурента.
Существенный недостаток этиленгликолевых растворов – их токсичность. Недопустимо их проникновение в грунтовые воды и в почву, особенно в местах, где используется грунтовая вода и выращиваются сельскохозяйственные культуры.
При неосторожном применении антифриз может попасть внутрь организма, что способно привести к летальному исходу. Материал также обладает сладковатым вкусом и не имеет неприятного запаха, а это создает повышенную опасность для животных и детей в случае протечек
Материал также обладает сладковатым вкусом и не имеет неприятного запаха, а это создает повышенную опасность для животных и детей в случае протечек.
Пропиленгликоль или этиленгликоль в отоплении?
Водные растворы пропилен гликоля не обладают токсичностью и подходят для использования в отопительных системах с высокими требованиями к экологичности: общественные и жилые постройки, фармацевтические, парфюмерные, косметические, пищевые производства и прочее. В таких инженерных схемах необходимо соблюдение экологической безопасности из-за риска проникновения антифриза в производимую продукцию и в производственные помещения.
Монопропиленгликоль предпочтителен для применения в системах отопления частных домов, коттеджных поселков, в местах, где используются грунтовые воды, почва или грунт для садов и огородов, сельскохозяйственных производств при опасности заражения продуктов и воды.
Несмотря на то, что по сравнению с этандиолом пропилен гликоль обладает большей вязкостью, теплоносители на его основе имеют «смазывающее» действие, улучшают функционирование насосов во вторичном контуре и способствуют удалению отложений с внутренних поверхностей теплообменного оборудования.
Этиленгликоль и пропиленгликоль: сравнение и выводы
Обобщив все вышесказанное, можно сделать вывод, что более высокие теплопроводность и теплоемкость этиленгликоля при его меньшей вязкости и доступной цене делают его предпочтительнее растворам на основе монопропиленгликоля. Но! Это правило действует только в тех случаях, где отсутствуют особые требования к экологичности теплоносителя.
Во всех остальных ситуациях необходимо использовать пропиленгликоль. Его отличия по теплофизическим свойствам от конкурента не столь существенны, но стоит он дороже. Хотя в данном случае это вопрос безопасности, на которой непозволительно экономить.
Теплоноситель этиленгликоль и пропиленгликоль: можно ли смешивать?
В связи с такой разницей в степени токсичности и в цене у многих возникает вопрос: можно ли смешать два спирта, чтобы получить не такой дорогой, как монопропиленгликоль, но менее токсичный, чем этандиол, аналог?
Ответ категоричен: жидкости не подлежат смешиванию, так как это, в лучшем случае, может привести к снижению характеристик более технологичного состава – пропилен гликоля, а в худшем вызовет образование осадка, так как растворы могут содержать присадки, несовместимые между собой. Поэтому следует выбрать только один из антифризов в соответствии с требованиями системы, а купить их по выгодным ценам можно у нас.